表观遗传学之 Chip-Seq
本文总阅读量 次
染色质免疫沉淀-测序(Chip-sequencing,简称 Chip-seq)用于分析蛋白质与 DNA 的交互作用。此技术结合了染色质免疫沉淀(Chip)和高通量 DNA 测序,旨在鉴定与 DNA 结合的蛋白质位点,从而精确绘制全基因组上目标蛋白的结合区域。在 Chip-seq 出现之前,Chip-on-chip 技术是研究蛋白质-DNA 相互作用的常用方法。
Chip(染色质免疫沉淀)技术被用于鉴定蛋白质与 DNA 的相互作用。因此,当前的 Chip-Seq 研究主要涉及两大类应用:转录因子的调控和组蛋白的修饰。
转录因子调控
在分子生物学中,转录因子(Transcription factor,TF)是能够结合在某基因上游 5’端特异序列上的蛋白质,它作为反式作用因子(能直接或间接地识别或结合在各类顺式作用元件核心序列上,参与靶基因转录效率调控的蛋白质或 RNA),与真核基因的顺式作用元件比如启动子、增强子等发生特异性相互作用,从而激活或者抑制基因的转录。
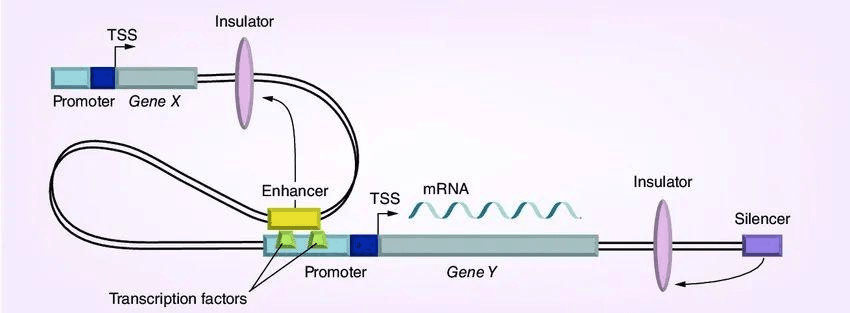
转录因子分为两类:通用转录因子和特异性转录因子。通用转录因子几乎在所有生物体细胞中都有存在。特异性转录因子在启动引发重大发育变化的基因表达模式中通常起着非常关键的作用。这些转录因子最显著的特点是都拥有 DNA 结合域,这使得它们能够与特定的 DNA 序列(称为增强子或启动子)上的 motif 结合。一些转录因子会与 DNA 上的启动子序列结合,靠近转录起始位点,从而帮助组装转录起始复合物。而其他转录因子则与调节序列,比如增强子序列,结合,它们能够刺激或抑制相关基因的转录活动。
解析转录因子如何与 DNA 互作以调节基因表达的过程对于深入理解多种生物过程和疾病状态至关重要。在此过程中,Chip-seq 技术能够发挥关键作用。
组蛋白修饰
染色质是指间期细胞核内由 DNA、组蛋白、非组蛋白及少量 RNA 组成的线性复合结构,是间期细胞遗传物质存在的形式。
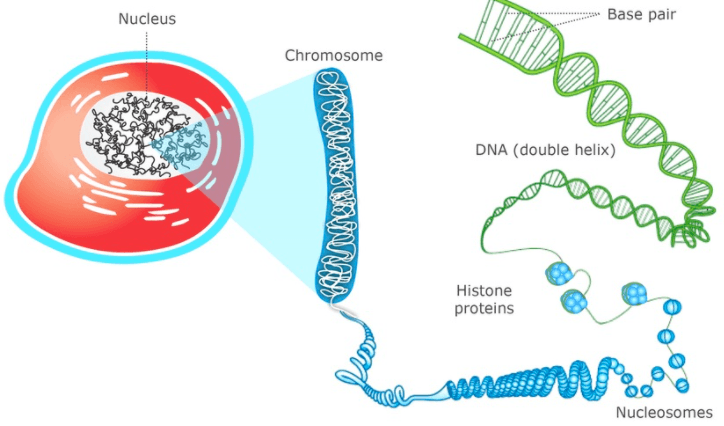
通过组蛋白特异性抗体,将带有特定修饰的组蛋白-DNA 复合物沉淀下来,从而获取组蛋白结合的 DNA,然后通过测序,可获得组蛋白在染色体上的分布情况,从而确定组蛋白修饰相关的特定位点,还可以确定组蛋白修饰酶类的靶标。Histone Chip-seq 一般与 ATAC-seq、RNA-seq 等一起联用。
利用特异性抗体识别组蛋白,可以沉淀带有特定修饰的组蛋白-DNA 复合物,进而提取出组蛋白结合的 DNA。通过进行测序分析,我们能够了解组蛋白在染色体上的分布模式,进而识别出组蛋白修饰的特定位点,并可能确定组蛋白修饰酶的作用靶标。Histone Chip-seq 一般与 ATAC-seq、RNA-seq 等一起联用。
组蛋白 N 端具有赖氨酸和精氨酸富集的尾巴,这些尾巴上的氨基酸可以被修饰酶添加不同的化学修饰,例如磷酸化、甲基化、乙酰化和泛素化等。这一过程被称为组蛋白修饰。在表观遗传学领域,组蛋白修饰对基因表达的调控起到关键作用,这种修饰属于蛋白质翻译后修饰(PTM),通过共价方式进行,包括甲基化(M)、磷酸化(P)、乙酰化(A)等。
- 组蛋白乙酰化与染色质的开放和转录激活密切相关
- 组蛋白甲基化涉及多种修饰类型和氨基酸残基,这些修饰既能激活转录(例如 H3K4me3、H3K36me3、H3K79me3),也能抑制转录(例如 H3K9me3、H3K27me3)
组蛋白包括 H2A、H2B、H3 和 H4 四种类型,其中“H”代表组蛋白,“K”代表赖氨酸位点,“me”表示甲基化修饰的个数,“ac”代表乙酰化修饰。
鉴于组蛋白修饰种类众多,我们在称呼组蛋白修饰时应遵循一定的命名规则:
组蛋白结构 + 氨基酸名称 + 氨基酸位置 + 修饰类型。
在实际应用中,通常这样表示:
- H3K4me3:代表 H3 组蛋白的第 4 位赖氨酸的三甲基化
- H3K27ac:代表 H3 组蛋白的第 27 位赖氨酸的乙酰化
组蛋白修饰应用于 Chip-seq 分析领域,有助于解析表观遗传特征和生物学功能。表观基因组学联盟提出的五个“核心组蛋白标记”在 Chip-seq 分析中得到了广泛应用:
- 与增强子区相关的 H3 赖氨酸 4 单甲基化(H3K4me1)或 H3 赖氨酸 27 乙酰化(H3K27ac)
- H3 赖氨酸 4 三甲基化(H3K4me3),与启动子区域相关
- H3 赖氨酸 36 三甲基化(H3K36me3),与基因体的转录区域相关
- 与 Polycomb 抑制相关的 H3 赖氨酸 27 三甲基化(H3K27me3)
- H3 赖氨酸 9 三甲基化(H3K9me3),与异染色质有关
详尽分析组蛋白修饰有助于更深入地理解发育和分化过程中的表观遗传机制。
ATAC-seq 和 Chip-seq
Chip-Seq 实验旨在验证一个特定的转录因子与 DNA 是否相互作用。在实验前,研究者已经确定了感兴趣的转录因子。通过设计针对该转录因子的抗体,进行 Chip 实验以捕获与之结合的 DNA 片段。这种方法有助于鉴定特定蛋白质与 DNA 之间的相互作用。
相比之下,ATAC-Seq 技术不针对特定的转录因子,而是用于检测全基因组范围内染色质的开放程度。通过这种技术,可以在全基因组水平上识别可能与蛋白质结合的位点。将 ATAC-Seq 与其他方法结合使用,可以帮助研究者筛选出感兴趣的调控因子。
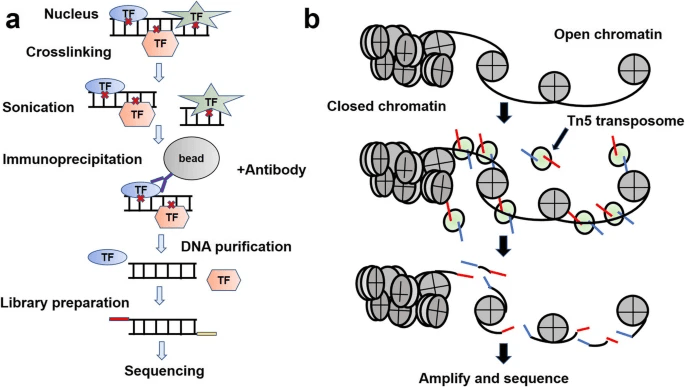
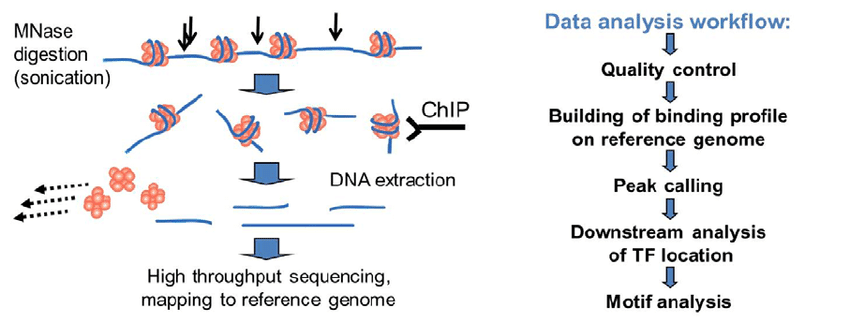
Chip-seq 的实验流程
Chip(染色质免疫沉淀)实验的基本步骤大致如下:
- 通过使用甲醛交联蛋白质和 DNA,确保它们结合,从而能够识别互作位点
- 采用超声波技术对 DNA 链进行片段化处理
- 进行染色质免疫沉淀,这是 Chip 实验的核心环节。通过使用特异性抗体捕获目标蛋白,形成 DNA-蛋白质复合物,并进行孵育和离心,以收集免疫沉淀物
- 对 DNA 进行回收和纯化,这包括断裂蛋白质和 DNA 之间的交联,并提取出纯净的 DNA
- 利用 qPCR 或 Chip 测序等分析方法对实验结果进行进一步分析
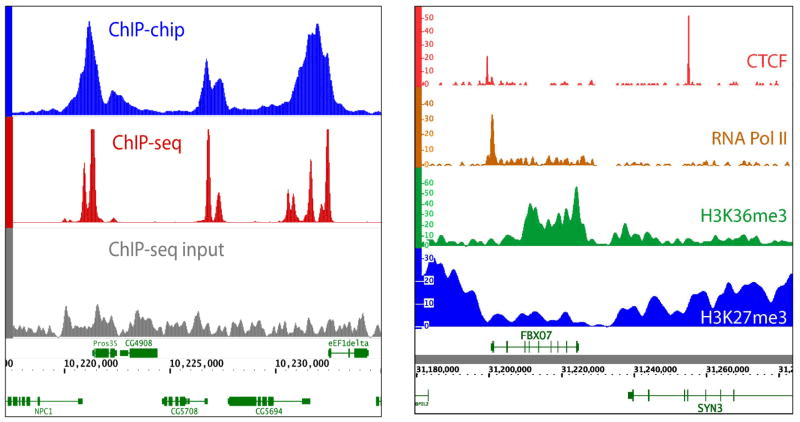
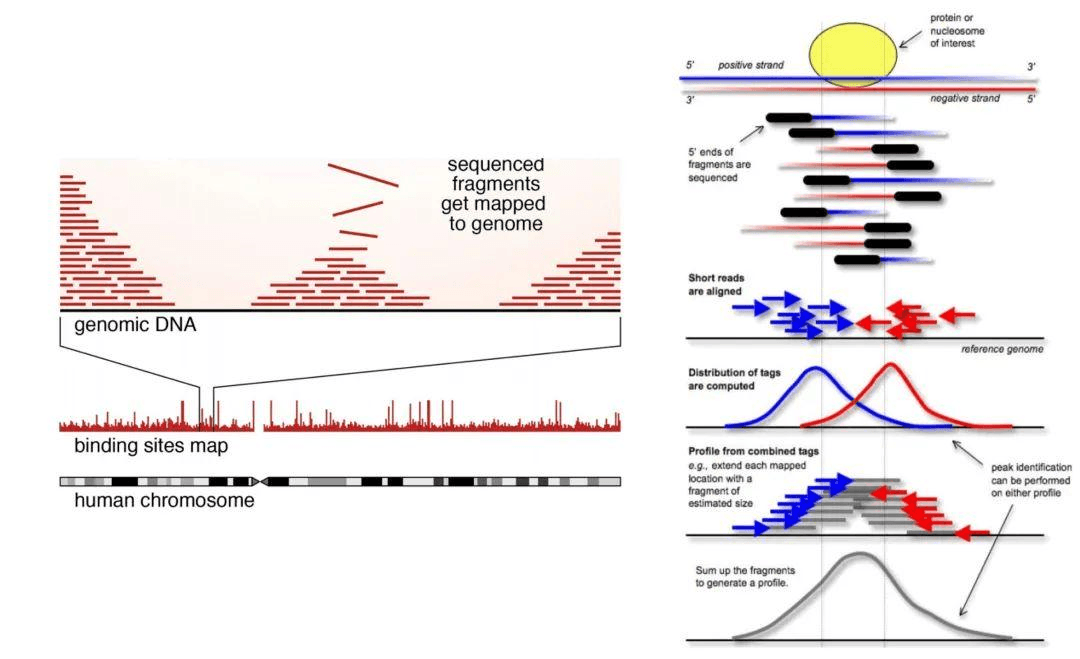
通过测序获得的 DNA 片段被映射到参考基因组上。实际上,这些 DNA 片段是随机的。当靶蛋白结合的片段数量增加时,测序得到的数据量也会增加。因此,在特定位置检测到的 DNA 片段堆叠高度会随之增加。相反,如果在该位置没有蛋白结合,DNA 片段堆叠就会非常低。这些 DNA 片段的堆叠被称作峰(Peak)。在下图中,红色和蓝色的箭头分别表示基因组中正链和负链的映射方向。将两个峰合并后,就能得到最终的峰。这样,我们就得到了文章中常见的 Chip-seq 峰图,其中 y 轴表示映射到的片段拷贝数,代表 Chip-seq 的信号强度,而 x 轴表示基因组坐标。
Chip-seq 的应用
- 确定蛋白质-DNA 结合位点:利用特异性抗体捕获蛋白质(例如组蛋白或转录因子),Chip-seq 能够揭示这些蛋白质在基因组上的结合区域
- 精确定位 RNA polymerase II 及转录因子结合位点:RNA polymerase II 是真核生物中负责转录蛋白质编码基因的主要酶,Chip-seq 有助于准确识别 RNA polymerase II 及其可能的同系物在基因组上的结合区域
- 探索组蛋白共价修饰与基因表达的关系:组蛋白是 DNA 在细胞核中的包装蛋白,其共价修饰(如甲基化、乙酰化等)会影响染色质的结构并调控基因表达,Chip-seq 可用于分析特定组蛋白修饰与基因表达调控之间的联系
- 研究转录因子结合位点:转录因子是调控基因表达的关键蛋白,Chip-seq 可用于识别和验证转录因子在基因组上的结合位点,进而揭示它们如何调控特定基因的表达模式
参考资料
- 一文讲明白 Chip-seq:高分文章里为什么做 Chip-seq?
- CHip-Seq 的概念、应用场景、原理、分析流程
- Integrative analysis of 111 reference human epigenomes
- Chip-seq 技术流程
- Profiling chromatin regulatory landscape: insights into the development of Chip-seq and ATAC-seq
- Transcription factors: an overview
- Chip-Seq: advantages and challenges of a maturing technology